第1节:磁共振成像中降噪的基本挑战
磁共振成像(MRI)是现代医学诊断的基石,提供了无与伦比的软组织对比度,而无需使用电离辐射。然而,获取MR信号的物理过程本质上容易受到噪声的影响,这一现象根本上限制了图像质量和诊断效用。噪声表现为像素强度的随机波动,这可能会遮蔽细微的解剖细节,模拟或掩盖病理,并破坏从图像中得出的定量测量。在解释MRI数据时,尤其是在功能性MRI(fMRI)等高级应用中,中心挑战在于辨别观察到的信号变化是否真实反映了潜在生理,还是仅仅是由噪声引起的随机波动。通过有效去噪来应对这一挑战并不是一项表面工作;而是实现更快、更高分辨率和更定量准确成像的关键步骤。为了开发和评估复杂的去噪算法,理解MRI噪声的物理来源和统计特征是至关重要的。
1.1. 噪声的物理学:热源和生理源
磁共振成像中的噪声是一个广泛的术语,指任何向测量的核磁共振(NMR)信号添加虚假波动的过程。这些波动源自扫描仪硬件、患者身体和周围环境中的多个来源。它们可以大致分为热源、生理源和系统相关源。
热噪声,通常称为约翰逊-奈奎斯特噪声,是一种基本且不可避免的信号降解源。它源于成像硬件和患者体内电子的随机热运动,这会在射频(RF)探测线圈中引发杂散电流。热噪声的主要来源是RF线圈本身的电阻、患者组织(样本)中的介电和感应损耗,以及首先接收MR信号的前置放大器的电子元件。这种噪声的特征是“白噪声”,意味着其功率谱是平坦的,并且均匀地破坏所获取信号的所有频率。这种噪声的大小与接收器带宽的平方根成正比;更宽的带宽允许更多的噪声进入每个体素的系统。
生理噪声源于受试者自身的生物过程。虽然热噪声在静态高分辨率解剖成像中通常是主要关注点,但在动态成像序列中,如功能性磁共振成像(fMRI)或心脏动态磁共振成像(心脏cine MRI),生理噪声常常成为主要的误差来源。其来源包括与心脏周期相关的脉动血流、导致胸部和腹部运动的患者呼吸,以及患者的自愿和非自愿运动。与热噪声的随机、无结构特性不同,生理噪声通常是准周期性的并且在空间上具有结构性,这使得其建模和去除特别具有挑战性。
系统相关噪声是指在MRI扫描仪操作过程中产生的 unwanted 信号。在现代超导扫描仪中,用于制冷系统的氦泵会产生一种持续的低频节奏“咚咚”声,即使在未进行主动扫描时也会存在。更为显著的是在扫描过程中产生的极其响亮的噪声。这些声音的音量可达到110-120分贝——相当于电锯——是由于大电流通过梯度线圈的快速切换所引起的。这些电流会产生强大的洛伦兹力,使线圈机械振动,辐射出声波。每个脉冲序列都有其独特的声学特征,基于其特定的梯度波形模式。虽然这种可听噪声主要是患者舒适度和安全性的问题,但潜在的机械振动和电磁干扰也可能导致图像质量下降。
可听系统噪声与统计图像噪声之间存在着重要的联系。最激进的脉冲序列,如回声平面成像(EPI),用于快速采集,如功能性磁共振成像(fMRI)和扩散加权成像(DWI),涉及最迅速和强烈的梯度切换,因此是最响的。这些快速序列本质上每单位时间获取的信号较少。图像的信噪比(SNR)与总采集时间的平方根基本成正比。因此,产生嘈杂和不适环境的脉冲序列设计也是那些产生最低内在SNR的图像,使其最容易受到热噪声和生理噪声的干扰。
1.2. 统计特征:从高斯分布到Rician分布
理解噪声的统计分布对于设计和验证去噪算法至关重要。原始MRI信号是在频域(k空间)中使用正交探测器获取的,该探测器测量信号的两个正交分量:实部和虚部。这些通道中的热噪声可以准确地建模为具有零均值的高斯分布。然后,通过二维傅里叶变换(2DFT)从这个复值k空间数据中重建图像。由于傅里叶变换是线性和正交的操作,它保留了噪声的高斯特性。结果是,在重建的复值图像中,实部和虚部的噪声都保持高斯分布,并且在整个视场内具有均匀的方差。
然而,绝大多数临床MRI图像并不是复数值的。为了避免与相位相关的伪影,临床医生通常查看幅度图像,这些图像是通过计算每个复数值像素的幅度生成的: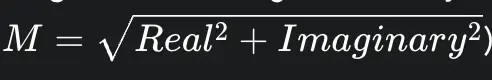
这看似简单的一步是一个非线性变换,根本上改变了噪声的统计特性。
在图像的区域中,当存在真实的NMR信号(即,在解剖组织内)时,结果幅度图像中的噪声不再遵循高斯分布。相反,它受Rician分布的支配。Rician分布的概率密度函数如下所示: 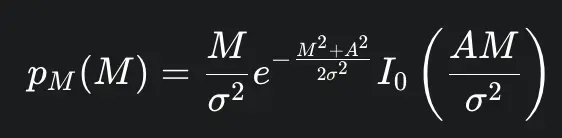
其中 M 是测量的像素强度,A 是真实的基础信号幅度,σ 是实部和虚部中原始高斯噪声的标准差,I0 是零阶第一类贝塞尔函数。瑞士分布是偏斜的,其形状取决于局部信噪比(SNR),定义为
A/σ。在高信噪比(SNR)下(当A≫σ时),瑞利分布接近高斯分布。然而,在低信噪比(例如,SNR < 2)时,分布明显非高斯且存在正偏差,这意味着测得的信号总是高于真实信号。
在图像中没有NMR信号的区域,例如患者外部的背景空气,真实信号A为零。在这种特殊情况下,Rician分布简化为Rayleigh分布。这是一个关键的区别,因为一种常见但有缺陷的做法是通过测量背景区域的标准差来估计图像噪声。这仅仅表征了Rayleigh噪声,并不能准确反映出感兴趣组织内存在的Rician噪声。
这种统计现实具有深远的影响。许多通用图像去噪算法,包括相当数量的早期深度学习模型,都是在假设简单的加性白高斯噪声(AWGN)的情况下设计和训练的。将这样的模型应用于包含信号依赖的Rician噪声的幅度MRI图像,代表了基本的模型不匹配。这可能导致次优性能、引入偏差以及细节的糟糕保留,特别是在Rician效应最明显的低信噪比(SNR)区域。这种不匹配是开发更复杂的、特定领域的人工智能模型的主要驱动因素,这些模型可以直接在幅度变换之前对复数值数据进行操作,或者明确设计用于处理Rician分布。
1.3. 噪声对诊断质量和定量分析的影响
磁共振成像(MRI)的最终目标是提供清晰的图像,以便进行准确的诊断和可靠的定量分析。噪声直接破坏了这一目标,因为它降低了图像质量,并减少了该质量的基本测量:信噪比(SNR)。低信噪比会妨碍放射科医生对图像的视觉解读,并降低对微妙病理的检测敏感性。
MRI扫描的信噪比(SNR)不是一个固定的属性,而是受到与硬件、采集协议和患者相关的复杂因素的影响:
磁场强度 (B0):开发高场 MRI 系统(例如,3T,7T)的主要动机之一是平衡磁化 (M0),即 MR 信号的来源,随着 B0 的增加而增加。这直接导致更高的潜在信噪比 (SNR)。
脉冲序列与对比度:脉冲序列参数的选择,如重复时间(TR)和回波时间(TE),会影响横向磁化,从而生成不同的组织对比度(例如,T1加权、T2加权)。这些操作本质上会影响采集时的信号幅度,从而影响最终的信噪比(SNR)。
采集时间和平均化:信噪比随着收集数据的总时间的平方根而改善。通过使用更长的采集窗口或平均多个采集(增加激发次数,或NEX)可以增加这一点。这在临床MRI中形成了中心权衡:更高质量的图像需要更长的采集时间,从而增加了成本和患者运动伪影的可能性。
空间分辨率(体素体积):实现高空间分辨率需要使用小体素。然而,体素的信号与其体积成正比。因此,较小的体素产生的信号较少,导致信噪比降低。
平行成像:像GRAPPA和SENSE这样的技术对于加速MRI扫描是不可或缺的。它们通过对k空间进行欠采样,并利用多个接收线圈的独特空间灵敏度特征来重建完整图像。虽然这大大减少了扫描时间,但代价是信噪比降低。重建过程会放大噪声,这一效应通过“g因子”来量化,并可能在最终图像中引入结构化的非均匀噪声模式。
除了简单的视觉退化,噪声对高级图像处理和定量分析有着恶劣的影响。在扩散张量成像(DTI)中,噪声会传播到估计的张量中,破坏组织微观结构的测量,如分数各向异性。对于高b值的扩散加权成像(DWI),这对于探测细微的微观结构细节至关重要,信号会严重衰减,剩余的低信号可能会被噪声完全淹没,从而偏倚所得到的测量结果。同样,噪声使得后续处理步骤,如图像配准,变得更加困难和不准确。因此,去噪不仅仅是美学上的改善,而是一项关键的使能技术,能够实现更快的扫描、更高的空间分辨率以及更稳健和准确的定量生物标志物提取。
第二节:去噪的演变:从经典滤波器到人工智能的曙光
去除图像噪声的探索与数字成像本身一样古老。几十年来,医学图像处理领域依赖于一套基于信号处理和统计原理开发的“经典”算法。这些方法为现代技术奠定了基础,并确立了去噪过程中涉及的基本权衡。然而,它们固有的局限性最终造成了性能的上限,为人工智能和深度学习带来的范式转变铺平了道路。
2.1. 传统方法概述:空间滤波、变换域和基于块的方法
传统去噪方法大致可以分为三类,每一类都代表着复杂性的增加。
空间滤波方法:这些是最直接的方法,在局部邻域内对受损图像的像素值进行操作。
线性滤波器:最简单的例子是高斯滤波器,它用邻域像素的加权平均值替换每个像素,权重遵循高斯分布。虽然在平滑噪声方面有效,但它无差别地模糊所有高频内容,包括锐利的边缘和细微的细节。
非线性滤波器:为了解决模糊问题,开发了非线性滤波器。例如,中值滤波器用邻域的中值替换一个像素,这对离群噪声更具鲁棒性。双边滤波器是一种更先进的边缘保留技术,它将空间域滤波与强度域滤波相结合。它对邻近像素进行平均,但每个邻居的权重不仅取决于其空间距离,还取决于其与中心像素的强度差异。这意味着它在平滑区域内进行平均,但在锐利边缘处停止平均。
各向异性扩散是另一种将去噪过程建模为热扩散方程的技术,它鼓励沿边缘平行的平滑,但抑制垂直于边缘的平滑。
变换域方法:这一类方法的原理是图像在变换域中可以更稀疏地表示。该过程包括三个步骤:1)对图像应用数学变换(例如,傅里叶变换、小波变换),2)操纵变换系数以抑制噪声,3)应用逆变换以返回图像域。
小波变换:由于其有效表示空间和频率信息的能力,这成为了一种基础技术。噪声往往在许多小波尺度上由小系数表示,而真实的图像结构则由少量大系数表示。通过对小波系数应用阈值(将小的系数设为零),然后反转变换,可以有效地去除噪声。
曲线变换和轮廓变换:这些是更高级的变换,旨在更好地捕捉图像中的曲线边缘和轮廓,而小波变换可能效率较低。
基于块(非局部)的方法:作为经典去噪的巅峰,这些算法建立在自相似的原则上——即任何给定的图像块通常在图像的其他地方有许多相似的对应部分。
非局部均值(NLM):由Buades等人提出,NLM滤波器通过在整个图像中搜索具有相似强度轮廓的其他补丁来对目标补丁进行去噪。然后,它计算这些相似补丁的加权平均值,以生成目标补丁的最终去噪结果。由于其在保留结构细节方面的有效性,NLM被广泛认为是一种优秀的MRI去噪技术。
块匹配与三维滤波 (BM3D):BM3D 是非局部均值 (NLM) 的一个有影响力且强大的扩展,它将补丁相似性的概念更进一步。首先,它找到相似的二维补丁并将它们堆叠在一起形成一个三维组。其次,它在三维变换域(如三维小波或离散余弦变换)中对该组应用协同滤波步骤,从而减弱噪声。最后,它反转变换并将去噪后的补丁聚合回图像的原始位置。多年来,BM3D 被认为是图像去噪的最先进技术,并且仍然是新方法比较的强大基准。
2.2. 固有限制:噪声减少与细节保留之间的权衡
尽管它们具有独创性,经典方法仍然存在几个根本性的局限性,这最终阻碍了它们在临床上的广泛应用,并促使人们转向基于学习的方法。
主要挑战在于噪声去除与保留诊断相关细节之间的持续而困难的权衡。更简单的滤波器不可避免地会导致模糊,不仅去除了噪声,还平滑了可能指示病理的细腻纹理和锐利边缘。虽然像NLM和BM3D这样的更先进的方法在边缘保留方面要好得多,但它们并不完美,仍然可能在复杂纹理或非常低的信噪比条件下遇到困难。
第二个主要障碍是计算成本。使得NLM和BM3D如此有效的机制——在图像中对相似补丁进行全面的非局部搜索——也是它们的致命弱点。这种搜索计算密集,使得这些算法非常缓慢,尤其是在处理大型3D MRI体积时。长时间的处理使得它们在常规临床放射科的快速工作流程中不切实际,因为重建和后处理必须迅速进行。这造成了一个关键的瓶颈:表现最佳的经典方法在临床使用中太慢。
其他局限性包括在滤波过程中引入新伪影的风险,这在临床上是不可接受的。[14] 此外,这些算法中有许多参数需要仔细手动调整以获得最佳性能,而最佳参数可能会根据图像对比度、解剖结构和噪声水平而显著变化,从而限制了它们的普适性。[21] 最后,虽然对像 AWGN 这样的简单噪声模型有效,但经典方法通常难以处理由现代加速技术(如并行成像)产生的复杂、空间变化和结构化的噪声。[10, 17]
这些经典方法的演变揭示了一条清晰的轨迹。由简单空间滤波器引起的模糊导致了变换域方法的发展,并最终发展到像 NLM 和 BM3D 这样的基于块的方法,它们在保留细节方面更胜一筹。然而,赋予 NLM 和 BM3D 强大功能的非局部搜索也使其计算成本过高。这造成了性能与速度之间的僵局,该领域难以克服。正是这个特定的瓶颈,深度学习恰好可以打破。虽然训练深度神经网络的计算成本很高,但一旦训练完成,推理步骤(对新图像进行实际去噪)可以在现代 GPU 硬件上极其快速地执行。[22] 因此,深度学习提供了一条可能达到或超过像 BM3D 这样的方法去噪性能的路径,但在推理时没有 crippling 的计算成本,直接解决了经典时代的关键局限性。
有趣的是,向人工智能的过渡并不意味着放弃最佳经典方法的核心原则。利用非局部自相似性的基本思想,这在 NLM 和 BM3D 中是核心,已被证明具有非凡的持久性。它已经演变并被整合到现代 AI 架构的结构中。早期的混合模型明确地结合了这两个世界,使用 CNN 来学习更好的相似性度量来指导传统的 NLM 滤波器。[22] 更深刻的是,最先进的 Transformer 模型核心的自注意力机制可以被看作是相同非局部比较概念的一种学习到的、动态的和数据驱动的实现。[21] 这展示了一个核心思想的复杂演变,而不仅仅是用一种新技术取代旧技术。
第 3 节:医学人工智能的主力:卷积神经网络架构
深度学习,特别是卷积神经网络(CNNs)的出现,标志着图像分析领域的一次革命性转折点。通过直接从数据中学习复杂的特征层次,CNNs 克服了经典的手工设计滤波器的许多局限性。它们迅速成为医学人工智能的主力,在去噪方面提供了最先进的性能,并构成了更先进模型所建立的架构基础。
3.1. 基础模型:DnCNN、U-Net 和自编码器
三种主要的 CNN 架构已成为 MRI 去噪领域的基础。它们的原理非常有效,以至于经常被用作更复杂、现代网络中的组件。
去噪卷积神经网络(DnCNN)是一个开创性的模型,它展示了一个相对较深的 CNN 在图像去噪方面的卓越效果。[11, 23] 它引入了两个成为该领域标准的关键概念。第一个是残差学习。DnCNN 不是训练网络将噪声图像直接映射到干净图像(f(y)→x),这可能是一个复杂的映射学习,而是学习预测残差噪声分量(f(y)→v)。然后通过从噪声输入中减去预测的噪声(x=y−f(y))可以轻松获得最终的干净图像。[7, 11] 这简化了优化问题并提高了性能。第二个创新是在卷积层之间使用批量归一化,这稳定了训练过程并允许使用更深的网络。[11, 23] DnCNN 架构本身是一个直接的卷积层级联,使其成为一个强大且被广泛引用的基准。[12]
自编码器(AEs)是学习高效数据编码的无监督神经网络。它们由两部分组成:一个将输入图像压缩成低维潜在表示的编码器,以及一个从这个压缩表示重建原始图像的解码器。[24] 压缩作为一个“信息瓶颈”,迫使网络学习图像最突出和最基本的特征,同时丢弃不太重要的信息,理想情况下包括噪声。使用卷积层进行编码器和解码器的卷积自编码器(CAEs)是图像去噪任务中常见且有效的变体。[24]
U-Net 架构,虽然最初是为生物医学图像分割设计的,但已成功地应用于图像恢复和去噪。[25, 26] 像自编码器一样,它具有对称的编码器-解码器结构,逐步下采样图像以捕获上下文,然后上采样以重建输出。其定义性特征是使用跳跃连接,它将编码器路径的特征图直接连接到解码器路径的相应层。[27] 这些连接为高分辨率空间信息提供了一条绕过瓶颈的捷径,使解码器能够以更高的保真度重建精细细节和锐利边缘。这种保留细节的能力使得 U-Net 架构非常适合去噪,其主要目标是在不模糊关键解剖结构的情况下去除噪声。[25, 26]
3.2. 架构创新和训练范式
在这些基础模型之上,研究人员开发了许多创新,以专门针对 MRI 数据的独特挑战定制 CNNs。
一个重要的步骤是从 2D 转向 3D 卷积。MRI 数据本质上是三维的,但早期的方法通常将其作为一系列独立的 2D 切片来处理。这未能利用相邻切片之间存在的强解剖相关性。通过使用 3D 卷积核,3D CNNs 可以一次性处理整个体积,从贯穿平面的维度学习特征,从而实现更稳健和准确的去噪,尽管计算成本更高。[22, 28]
另一个关键的创新是复数值网络的开发。如前所述,标准 CNNs 在幅度图像上操作,这丢弃了有价值的相位信息,并迫使网络学习复杂的、非高斯的莱斯噪声分布。为了克服这个问题,一些模型被设计为直接在扫描仪的原始复数值数据上操作。[8, 9] 这些网络使用复数值的权重、卷积和激活函数。通过在复数域工作,它们可以利用幅度和相位信息,并且可以在更简单、更易于理解的高斯噪声模型上进行训练,这已被证明可以带来卓越的性能,特别是在处理并行成像引入的空间变化噪声方面。[8]
CNNs 内部的架构演变揭示了一个一致的模式,即识别并重新整合在简单处理流程中丢失的信息。标准自编码器在其瓶颈处丢失了高频细节,因此 U-Net 添加了跳跃连接以带回这些信息。2D CNN 丢失了体积上下文,因此开发了 3D CNN 来整体处理体积。在幅度图像上操作的标准 CNN 丢失了相位信息,并且必须应对莱斯噪声,因此创建了复数值 CNN 以处理原始的、完整的数据。这展示了朝着构建更能充分感知 MRI 数据原生结构的模型迈出的清晰而合乎逻辑的进展。
这些模型的主要训练范式是监督学习,它需要一个大型的配对数据集,包括噪声输入图像和“干净”的真值目标图像。[10, 22] 然而,“真值问题”是 MRI 中的一个根本挑战:在实践中,真正无噪声的图像是不存在的。[9, 22] 因此,研究人员必须创建/代理/真值。这通常通过两种方式之一完成:1)采集具有非常高信号平均次数(高 NEX)的图像,这虽然耗时,但能产生高信噪比的参考图像 [11, 29],或者 2)获取高质量图像,并计算上添加模拟的高斯或莱斯噪声以创建噪声输入对。[22, 29] 对代理真值的依赖是一个关键点;这意味着监督模型通常学习的是逆转一个特定的、可能简化的噪声模型。这可以解释为什么它们有时难以泛化到在真实临床扫描中遇到的复杂和非平稳的噪声模式。[8]
3.3. 临床环境中的性能和局限性
在性能方面,基于 CNN 的方法已被证明取得了巨大的成功,始终优于经典算法。大量研究表明,与 BM3D 等传统滤波器相比,CNNs 在峰值信噪比(PSNR)和结构相似性指数(SSIM)等量化指标上取得了显著更高的分数。[24, 28] 例如,一项比较各种 3D 去噪方法的合成和真实数据研究发现,一种提出的多通道 3D CNN 在真实数据上实现了 38.16 的 3D PSNR,大大超过了经典最先进的 BM4D 算法实现的 35.58。[28]
基于 CNN 的去噪最显著的临床影响是其实现更快扫描的能力。通过有效去除噪声,这些算法可以补偿因加速采集技术而发生的信噪比损失。这允许使用更少的信号平均次数(更低的 NEX)或更高的并行成像加速因子,从而在保持甚至提高图像质量的同时,显著减少扫描时间。[10, 11, 12, 20] 这对患者舒适度、扫描仪吞吐量和减少运动伪影具有深远的影响。
尽管取得了这些成功,CNNs 并非没有局限性。它们的性能高度依赖于训练数据;它们是数据饥渴的,模型的有效性受到其训练数据集的大小、多样性和质量的限制。[17, 23] 这导致了泛化性和领域漂移的关键问题。一个仅在西门子 3T 扫描仪的 T1 加权脑部扫描上训练的模型,在 GE 1.5T 扫描仪的 T2 加权膝关节图像上可能表现不佳。[30] 这种在不同扫描仪、解剖结构和成像对比度之间缺乏鲁棒性是广泛临床部署的主要障碍。此外,虽然 CNNs 在保留细节方面比经典滤波器更好,但如果学习到的滤波器适应性不足,它们仍然可能在结构非常复杂的区域(如小脑)引入微妙的模糊。[11] 最后,也是最关键的是,一个训练不佳或泛化不当的模型存在产生新的、微妙的伪影的风险,这些伪影可能被误认为是病理,或者相反,通过将真实的病理特征误解为噪声而将其移除。[10, 14]
第 4 节:用于高保真图像恢复的生成模型
虽然标准 CNNs 学习从噪声图像到干净图像的直接映射,但一类更强大的模型,即生成模型,学习数据本身的潜在分布。这使它们能够生成新的、高度逼真的图像内容。两种类型的生成模型主导了最近的 AI 研究,并正在积极探索用于 MRI 去噪:生成对抗网络(GANs)和去噪扩散概率模型(扩散模型)。这些模型可以产生视觉上令人惊叹的结果,但也伴随着一系列独特而关键的风险,在临床环境中必须仔细考虑。
4.1. 对抗性方法:使用生成对抗网络(GANs)进行去噪
GANs 引入了一种基于竞争的新颖训练范式。[31] GAN 框架由两个在零和博弈中相互对抗的神经网络组成:
生成器网络将噪声图像作为输入,并试图生成一个逼真的、去噪后的版本。其目标是创建一个与真实的、高质量的 MR 图像无法区分的输出。[26, 32]
判别器网络作为对手。它被训练来区分生成器产生的“假”图像和“真”的高质量基准图像。[31, 32]
训练过程是一个迭代循环。判别器关于哪些图像看起来是假的反馈被用来更新生成器的参数,教它产生更具说服力的假图像。同时,生成器日益复杂的假图像被用来训练判别器成为一个更好的检测器。[32] 这种对抗性动态迫使生成器不仅学习图像的像素级内容,还学习使它们在挑剔的观察者看来具有感知真实性的微妙纹理、边缘和统计特性。[33]
在架构上,生成器通常基于 U-Net 或其他编码器-解码器结构,而判别器通常是标准的分类 CNN。[26] 用于训练 GANs 的损失函数是一个关键组成部分,通常结合传统的像素级重建损失(如 L1 或 MSE)以确保保真度,以及从判别器输出中导出的对抗性损失。这个对抗性分量惩罚生成器产生被判别器识别为假的图像,从而推动结果向更高的真实性发展。[26, 34]
4.2. 迭代方法:使用扩散模型进行去噪
扩散模型是最近出现的一类更强大的生成模型,在图像合成方面取得了最先进的成果。[35] 它们基于一个渐进的两步过程:
前向扩散过程: 这是一个固定的过程,在训练期间,通过在大量离散时间步的每一步中逐渐添加少量高斯噪声来逐步破坏干净的图像。经过数百或数千步后,原始图像被转化为纯粹的、非结构化的噪声。[36]
反向去噪过程: 然后,模型(通常是类似 U-Net 的架构)被训练来逆转这个过程。在每个时间步,它学习预测并移除添加的少量噪声,从而向干净图像迈回一步。[36]
在推理过程中,去噪过程从噪声 MRI 图像开始。模型估计噪声水平,然后多次迭代应用学习到的反向步骤,逐步细化图像并去除噪声,直到产生干净的输出。[36] 这种迭代细化过程使扩散模型能够生成具有卓越细节和对学习数据分布高度保真度的图像。
4.3. 一个关键问题:生成具有临床误导性的合成结构的风险
生成模型的强大之处也正是它们在医疗领域中最大风险的来源:幻觉的潜力。因为这些模型学习真实图像的分布,它们在“填补”统计上合理的细节方面变得异常出色,即使这些细节实际上并未得到输入信号的支持。这可能表现为生成原始噪声数据中不存在的合成结构或纹理。[36]
这不是一个理论上的担忧。在 2024 年 MICCAI 会议上发表的一篇关于应用于医学图像去噪的扩散模型的批判性分析明确调查了这一风险。[36] 该研究得出了两个令人担忧的结论。首先,作为扩散模型标志的迭代采样过程实际上可能在标准指标方面降低图像质量,PSNR 与简单的一步去噪相比下降高达 14%。其次,更重要的是,该研究提供了视觉证据,表明采样过程的随机性可能引入对图像内容的改变,生成合成结构,从而损害去噪图像的临床有效性。[36] 另一项关于基于扩散的 MRI 重建的研究发现,这些模型容易受到微小的、最坏情况下的扰动的影响,这些扰动可能导致它们生成假的组织结构,这可能会灾难性地误导临床医生。[37]
GANs 虽然不像扩散模型那样容易出现迭代退化,但也面临着自身的挑战。它们的训练是出了名的不稳定,可能会遭受“模式崩溃”,即生成器学会只产生有限种类的输出,而不管输入如何。[35, 38]
这在医学成像 AI 的发展中造成了一种根本性的张力。一方面,人们渴望获得具有锐利边缘和逼真纹理的感知上高质量的图像,而生成模型在这方面表现出色。[34, 39] 另一方面,绝对需要诊断保真度——保证去噪后的图像是所采集信号的真实再现。一个用像素级损失函数训练的简单 CNN 可能会产生一个稍微模糊但更忠实的图像,因为它会因任何偏离基准真值的行为而受到严重惩罚。一个 GAN 或扩散模型可能会产生一个更清晰、更具视觉吸引力的图像,并获得高 SSIM 分数,但代价是可能对底层数据不那么真实。因此,“最佳”算法不仅仅是在给定指标上得分最高的算法,而是在这些相互竞争的目标之间达到最临床上适当和安全平衡的算法。纯数据驱动的生成模型所带来的重大风险,是开发新范式(如物理信息 AI)的主要动机,这些新范式可以利用它们的力量,同时约束它们的行为,以确保临床安全性和可靠性。
第 5 节:新先锋:基于 Transformer 的架构
近年来,一种名为 Transformer 的新型神经网络架构从自然语言处理领域崛起,并开始挑战 CNNs 在计算机视觉领域的主导地位。通过采用强大的自注意力机制,Transformers 能够比 CNNs 更有效地建模数据中的长程依赖关系。当应用于医学成像时,这些模型展示了最先进的性能,尤其是在最具挑战性的低信噪比场景中,使它们成为追求高保真 MRI 去噪的新先锋。
5.1. 为医学成像调整注意力机制(例如 SwinIR, Imaging Transformer)
Transformer 的核心创新是自注意力机制。对于图像中的任何给定块(或“令牌”),自注意力会动态计算一组“注意力分数”,这些分数衡量图像中所有其他块对于解释当前块的重要性。这使得模型能够通过明确建模图像遥远部分之间的关系来构建一个丰富的、上下文感知的表示,克服了 CNN 卷积核固有的局部感受野的限制。[21, 23, 40]
为高分辨率图像调整这种强大的机制已导致了几个关键的架构发展:
Swin Transformer: 标准的 Vision Transformer (ViT) 通过将图像分解为一系列块并应用全局自注意力来处理图像,这在计算上是昂贵的。Swin (Shifted Window) Transformer 通过首先仅在局部的、不重叠的窗口内计算自注意力来使此过程更高效。然后,它通过在后续层中移动窗口网格来实现跨窗口通信。这种分层方法提供了全局上下文建模的好处,同时保持了相对于图像大小的线性计算复杂性,使其在视觉任务中变得实用。[41, 42]
SwinIR: 该模型是基于 Swin Transformer 构建的通用图像恢复任务的强大基准。[43] 其架构包括三个主要部分:一个浅层特征提取模块(通常使用 CNNs),一个由多个残差 Swin Transformer 块(RSTBs)组成的深层特征提取模块,以及一个最终的高质量图像重建模块。SwinIR 在标准去噪基准测试中展示了最先进的性能。[42]
Imaging Transformer (IT): 这是由微软研究院专门为 MRI 去噪开发的一种高度专业化和强大的架构。[44, 45] 它代表了 CNN 和 Transformer 世界最佳思想的复杂综合。它使用高分辨率网络(HRNet)作为其骨干,以在整个网络中保持高分辨率特征图——这一概念在 CNNs 中已被证明是有效的。嵌入在该骨干中的是新颖的 IT 块,它将注意力机制分解为三个专门的模块:空间局部注意力、空间全局注意力和帧(或时间)注意力。这种设计使其能够处理 5D 张量(批次、通道、帧、高度、宽度),使其在处理 2D、3D 和动态(2D+T)MRI 数据方面具有单一统一架构的非凡通用性。[44, 45]
5.2. 在极低信噪比场景下的可扩展性和性能
基于 Transformer 的模型,特别是在具有挑战性的条件下,其性能非常出色。研究一致表明,像 SwinIR 和 IT 这样的架构显著优于强大的 CNN 甚至其他 Transformer 基准模型。[42, 45, 46]
它们强大能力的最有力证据来自于它们在极低信噪比环境下的表现。微软的 Imaging Transformer (IT) 在输入信噪比低至 0.2 的电影 MRI 数据上进行了测试,在这种水平下,原始图像完全被噪声掩盖,临床上无法解读。该模型能够恢复出具有清晰解剖细节的高质量图像。至关重要的是,这不仅仅是外观上的改善;两位资深心脏病专家的定性审查证实,去噪后的图像提供了与高信噪比基准图像相同的临床解释。此外,从去噪图像中得出的左心室射血分数(EF)等定量测量值与基准值相比是准确的。[44, 45]
这种能力对 MRI 的未来具有深远的影响。Transformers 在信噪比远低于 1 的输入中产生临床有效结果的能力,可能会从根本上改变 MRI 硬件的格局。它为低场强 MRI(例如 0.55T 系统)打开了大门,这种系统本质上比高场强系统更便宜、更小、更易于普及,从而成为广泛临床应用的可行替代方案。[47, 48] 通过计算补偿这些系统固有的低信噪比,先进的 AI 去噪可以使 MRI 技术民主化,特别是在资源不足或即时护理环境中。
IT 架构还展示了出色的可扩展性。以 SSIM 和 PSNR 衡量的性能随着模型大小从 2700 万增加到 2.18 亿参数而持续提高,这表明其具有从海量数据集中学习复杂噪声模式的高容量。[44, 45] 随后在一项相关的“imformer”模型上的工作,该模型使用了一种新颖的“SNR 单元”训练方案,显示出在不同扫描仪场强、成像对比度和解剖区域之间的强大泛化能力,解决了临床转化的一个关键挑战。[49]
5.3. 相对于基于 CNN 方法的比较优势
在图像去噪方面,Transformers 相对于纯粹基于 CNN 的方法具有几个关键优势:
全局上下文建模: 如前所述,它们建模长程依赖关系的能力使它们能够理解解剖结构的全局结构,并捕获超出 CNN 固定大小核范围的非局部噪声相关性。[23, 40]
基于内容的动态操作: 自注意力权重是根据图像内容本身动态计算的。这可以被解释为一种更强大、更灵活的空间变化卷积版本,其中“滤波器”会适应图像中的局部结构。[42]
参数效率: 像 SwinIR 这样的模型已被证明在性能上更优,同时使用的参数明显少于竞争的 CNN 模型,这表明它们对去噪任务的表示更为高效。[42]
然而,最先进研究的趋势不一定是将 CNNs 完全替换为 Transformers,而是开发强大的混合模型,利用两者的优势。像 SwinMR 和 RepCHAT 这样的模型在网络的浅层和深层使用 CNN 层进行高效的局部特征提取,同时使用基于 Transformer 的骨干来处理复杂的全局特征整合。[40, 50] 这表明 CNNs 对局部模式的归纳偏置和 Transformers 的全局上下文建模是高度互补的,它们的结合代表了当前架构设计的前沿。[21]
第 6 节:稳健和数据高效去噪的新范式
尽管 CNNs 和 Transformers 的架构创新推动了性能的边界,但两条平行且同样重要的研究路线则专注于从根本上改变模型的训练方式。这些新兴的范式——自监督学习和物理信息学习——直接解决了标准监督式 AI 最关键的瓶颈:对海量、完美策划的数据集的依赖,以及缺乏固有的鲁棒性和信任度。
6.1. 自监督学习:打破对干净基准数据的依赖
在开发医学成像 AI 方面,最大的实际挑战是“基准数据问题”。标准的监督学习需要大量的配对数据集,包括噪声输入图像和完美的干净目标图像。[22] 正如已经确立的,获取真正无噪声的 MRI 数据在物理上是不可能的,这使得创建这样的数据集不切实际,并迫使研究人员依赖不完美的替代品。[9, 16, 51]
*自监督学习(SSL)*是一种范式转变,它通过仅使用噪声数据本身来训练模型,从而巧妙地回避了这个问题。[52, 53] 这些方法通过利用噪声的统计特性和图像数据中固有的冗余性来工作。已经开发了几种关键技术:
Noise2Noise (N2N): 这种方法需要对同一场景进行两次独立的噪声采集。网络被训练来将一个噪声图像映射到另一个。因为两个图像中的潜在解剖信号是相同的,但随机噪声是不相关的,所以网络最小化误差的最佳策略是学习真实的、潜在的干净信号。[51] 将 N2N 应用于 MRI 的主要挑战是,两次所需扫描之间的患者运动难以避免,这违反了静态潜在场景的假设。[9]
盲点网络: 这是一种更实用且广泛使用的 SSL 方法家族,仅需要单个噪声图像。其核心思想是训练网络仅根据其周围邻居来预测给定像素的值,而中心目标像素在该预测中被人为地“屏蔽”或从网络的感受野中排除。由于给定像素处的噪声通常与其邻居处的噪声在统计上是独立的,网络不能简单地学习一个恒等映射。为了做出准确的预测,它被迫从邻近像素提供的上下文中学习潜在的解剖结构。[16] 这种方法的著名例子包括 Noise2Void (N2V) 和 Self2Self (S2S)。[52]
斯坦无偏风险估计器(SURE): 这是一个统计框架,允许网络使用一个损失函数进行训练,该函数提供了对干净基准数据的真实均方误差的无偏估计,即使从未见过该基准数据。它有效地允许在没有监督数据的情况下进行监督式训练。[16, 54]
这些方法的性能令人印象深刻。最近一项关于多维自监督技术(MD-S2S)的研究表明,与 BM3D 等经典方法以及 Patch2self 等其他 SSL 方法相比,它极大地提高了去噪性能。至关重要的是,它还显著提高了从去噪图像中得出的下游定量参数图的准确性。[52, 53] SSL 代表了一种变革性的方法,它使稳健、数据高效的深度学习在配对数据稀缺的更广泛临床应用中变得可行。
6.2. 物理信息神经网络(PINNs):整合物理先验以增强鲁棒性
对纯数据驱动的 AI 模型的一个主要批评是,它们可能作为“黑箱”运行,可能会从训练数据中学习到虚假的关联,或者产生虽然视觉上看似合理但违反已知物理定律的输出。*物理信息神经网络(PINNs)*通过将底层物理过程的领域知识明确整合到学习框架中来解决这个问题。[55, 56, 57]
在 MRI 去噪的背景下,这通常是通过向网络的目标函数添加一个基于物理的损失项来实现的。如果网络的输出与已知的 MR 信号行为物理模型不一致,该项就会对网络进行惩罚。例如:
在*弥散加权成像(DWI)*中,已知信号强度会随着 b 值的增加而呈指数衰减。为 DWI 去噪设计的 PINN 可以包含一个损失项,以确保在多个 b 值下去噪后的信号强度遵循这一物理模型。这不仅可以规范化网络以防止幻觉,还有助于保持衍生参数(如表观弥散系数 ADC)的定量准确性。[58]
在MRI 重建和伪影校正中,PINNs 可以被成像形成本身的物理学所告知。可以使用数据一致性损失项来确保去噪图像的 k 空间表示与最初采集的(尽管有噪声和欠采样)k 空间数据保持一致。[57, 59, 60]
这种方法的结果非常令人鼓舞。一项 2025 年关于高 b 值 DWI 去噪的 PINN(名为PIND)的研究报告了出色的性能。它将 PSNR 从 31.25 dB 提高到 36.28 dB,SSIM 从 0.77 提高到 0.92。最重要的是,它在保持定量 ADC 值 98% 的准确性的同时,实现了潜在的83% 的扫描时间缩减。[58] 这表明 PINNs 可以在不牺牲数据定量完整性的情况下实现出色的降噪,这是临床转化的关键要求。
自监督学习和物理信息学习的兴起可以被看作是一种趋同进化。这两种范式从根本上都是为了解决同一个核心挑战:当完美的基准数据不可用时,图像恢复的病态性质。它们通过引入强大的正则化形式来约束巨大的解空间来实现这一目标。自监督学习增加了一个统计约束,强制在噪声数据本身内部保持一致性。PINNs 增加了一个物理约束,强制与成像模式的已知定律保持一致性。它们代表了通往同一目标的两条不同但互补的路径:创建更智能、更稳健、更值得信赖的 AI 模型,这些模型对不可能获得的大量完美数据集的依赖性更小。这一趋势是对临床界对“黑箱”AI 合理怀疑的直接回应,对于弥合实验室研究与现实世界临床应用之间的差距至关重要。
6.3. 混合模型:结合经典和基于 AI 方法的优势
虽然研究的重点已大量转向端到端的深度学习,但一种务实且高效的方法是创建混合模型,将 AI 的优势与经典算法的成熟原理相结合。这种方法不是将经典方法视为过时,而是将它们视为可以通过深度学习增强的强大先验。
最早成功的混合策略之一是使用AI 引导的经典滤波器。在这种两阶段方法中,首先使用 CNN 生成一个初步的、预滤波的图像。这个输出虽然不完美,但比原始的噪声输入更能估计干净的图像。然后,这个预滤波的图像被用作传统 NLM 或 BM3D 滤波器中的“引导图像”。通过为块相似性搜索提供更好的参考,CNN 显著提高了经典滤波器的性能,从而获得了优于任何一种方法单独所能达到的结果。[22, 61] 这种方法还有助于减轻有时由基于块的 CNNs 产生的块状伪影。[22]
另一种混合方法涉及将 AI 与变换域方法相结合。例如,开发了一种用于 CT 去噪的方法,该方法首先应用非下采样剪切波变换,然后使用 DnCNN 作为后处理步骤,以清除变换域滤波后残留的任何噪声。[62] 这些混合模型有力地提醒我们,数十年来在经典图像处理方面的研究已经产生了宝贵的工具和概念,这些工具和概念可以被智能地整合,而不是简单地被现代深度学习技术所取代。
第 7 节:性能比较分析
确定“最佳”AI 去噪方法需要进行多方面的评估,而不仅仅是单一的性能指标。它涉及对定量基准、定性临床效用、特定模态性能以及计算成本等实际考虑因素的批判性评估。尽管研究领域分散,使得进行明确的、全面的比较具有挑战性,但从现有证据中可以清楚地看到性能的层级和一系列关键的权衡。
7.1. 定量基准测试:评估 PSNR、SSIM 及其他关键指标
评估去噪算法最常用的客观指标是峰值信噪比(PSNR)和结构相似性指数(SSIM)。[14, 56] PSNR 是基于均方误差(MSE)的像素级重建误差度量,而 SSIM 则旨在更好地与人类对结构信息、亮度和对比度的感知保持一致。[63, 64]
根据这些指标,可以从文献中建立一个清晰的性能层级:
深度学习 > 经典方法: 在众多研究中,深度学习模型始终且显著地优于即使是最先进的经典方法,如 BM3D 及其三维变体 BM4D。例如,在一项对 3D 去噪方法的直接比较中,一个提出的多通道 3D CNN 在真实 MRI 数据上实现了 38.16 的 3D PSNR 和 0.9924 的 3D SSIM,而最先进的经典方法 BM4D 分别只达到了 35.58 和 0.9882。[28]
高级 DL 架构 > 简单基准: 在深度学习生态系统中,更先进的架构通常优于简单的架构。包含捕捉长程信息机制的模型,如 Transformers(例如 SwinIR)或具有 U-Net 结构和非局部模块的 CNNs,相比于纯前馈 CNN 结构(如原始的 DnCNN),显示出显著的改进。[65] 基于 Transformer 的模型,如 Imaging Transformer,也已被证明优于其他 CNN 和 Transformer 基准。[45]
下表是从一项关于 3D MRI 去噪的比较研究中综合得出的,提供了在真实数据上这一层级结构的具体证据。[28] “3D-Proposed”模型是一个多通道 3D CNN。
表 1:真实 3D MRI 数据上的定量性能基准
| 指标 | 输入 | BM4D (经典) | 3D-DnCNN | 3D-EnsembleNet | 3D-Proposed |
| 3D PSNR | 34.77±2.12 | 35.58±1.88 | 37.92±2.15 | 37.98±2.00 | 38.16±2.45 |
| 3D SSIM | 0.9852±0.0054 | 0.9882±0.0038 | 0.9918±0.0030 | 0.9921±0.0028 | 0.9924±0.0030 |
然而,认识到这些指标的局限性至关重要。PSNR 和 SSIM 并不总是与诊断效用相关。一个过度平滑图像的算法可以获得高 PSNR,而一个产生看似合理但虚假细节的生成模型可以获得高 SSIM。[36, 63] 这种“基准幻觉”是该领域的一个系统性挑战;由于没有单一的、普遍接受的基准数据集或评估协议,跨不同论文比较结果可能会产生误导。[30, 66] 在一项研究中表现最先进的模型,在不同解剖结构或与其他竞争模型进行测试时可能会表现不佳。这强调了定性评估和开发更具临床相关性评估指标的必要性。
7.2. 特定模态性能:T1 加权、T2 加权和弥散加权成像(DWI)
最佳的去噪策略可能因特定的 MRI 序列而有显著差异,因为每个序列都因其对比度机制和噪声特性而带来独特的挑战。
T1 和 T2 加权成像: 对于标准的解剖成像,深度学习重建(DLR)已被证明是广泛有效的。对使用 T1 和 T2 加权序列的儿科身体 MRI 的研究发现,DLR 显著改善了信噪比和对比度噪声比,从而导致放射科医生给出的总体图像质量评分高于传统重建。[67]
定量 T1 映射: 这种先进技术提供了组织健康的定量生物标志物,但对噪声敏感。一项评估用于心肌 T1 映射的超分辨率 DLR(SR-DLR)的研究发现,它没有改变平均 T1 值(保持了定量准确性),但显著降低了测量的标准差。这表明 DLR 方法提高了 T1 映射的精度和可靠性,而没有引入偏差。[68, 69]
弥散加权成像(DWI): DWI 可谓是去噪中最具挑战性和最重要的模态。DWI 中的信号固有地很低,特别是在探测组织微观结构所需的高 b 值下,使其极易受到噪声的影响,噪声可能淹没信号并使定量测量产生偏差。[13] 因此,已经为 DWI 开发了许多专门的 AI 方法。一个简单的 1D-CNN,沿弥散编码维度逐个体素应用,被证明是高 b 值 DWI 的一种有效方法,克服了其他方法(如 Marcenko-Pastur PCA (MP-PCA))的局限性。[13] 像 Noise2Noise 这样的自监督方法也已成功应用,从而避免了对干净基准数据的需求。[51] 最有希望的是,像 PIND 这样的物理信息模型,利用已知的弥散物理学,已证明在保持定量 ADC 图谱高保真度准确性的同时,具有出色的降噪效果。[58]
这一分析强调,虽然通用去噪器可能有效,但像 DWI 和 T1 映射这样最具挑战性和定量敏感性的模态,通常受益于专门为处理其独特信号特性和保持其定量完整性而设计的 AI 解决方案。
7.3. 定性评估:放射科医生评估在确定临床可行性中的作用
虽然定量指标提供了数学保真度的衡量标准,但算法成功的最终仲裁者是其临床效用,这只能通过专家人类观察者的定性评估来确定。只有当去噪后的图像能够改善,或者至少不妨碍放射科医生做出准确诊断时,它才是有用的。
许多高质量的研究将读者研究作为其验证过程的关键组成部分。例如:
一种用于加速脑部 MRI 的 AI 方法由五位经委员会认证的放射科医生进行评估,他们证实 AI 增强的图像保留了关键病理特征的可见性。[25]
Imaging Transformer 模型由两位资深心脏病专家验证,他们一致认为,即使是从极度嘈杂的输入中,其输出也提供了与基准图像相同的临床解释。[44, 45]
一项涉及四位放射科医生的读者研究证实,用于 DWI 的 PIND 模型在总体图像质量、伪影抑制和病灶显眼度方面表现出有希望的性能。[58]
放射科医生的评估对于识别 AI 的失败模式也至关重要。一位专家放射科医生能够识别出使用 MSE 成本函数训练的网络导致图像过度平滑,从而促使研究人员转向更有效的 MAE 损失函数。[70] 这强调了仅靠定量指标不足以进行模型开发和验证。任何去噪算法的临床转化绝对需要放射科医生进行严格的、在环验证,以确保最终的图像不仅视觉上吸引人,而且在诊断上是安全和有效的。
7.4. 计算成本和推理时间:部署的实际考虑
要将 AI 算法整合到临床工作流程中,它必须在计算上是高效的。深度学习相对于 BM3D 等先进经典方法的一个关键优势是训练和推理的分离。虽然训练一个深度网络可能需要数小时或数天,但推理过程——将训练好的模型应用于新图像去噪——通常非常快,在 GPU 上通常只需几秒钟或更短时间。[22]
然而,并非所有 AI 模型在计算成本方面都是相同的。模型复杂性与效率之间存在明显的权衡。一项对不同 DL 模型的比较研究发现,一个更简单的噪声到干净(N2C)网络在计算上最有效,而一个更复杂的 CycleGAN 效率最低。[71, 72] 在 3D CNNs 中,一个多通道架构被证明比标准的 3D-DnCNN 具有更少的可训练参数和更低的计算要求(FLOPs),同时实现了更好的性能。[28] 扩散模型是一个显著的例外;它们的迭代采样过程使其推理时间明显长于单次通过模型(如 CNNs 或 Transformers),这是其临床部署的一个主要实际障碍。[36] 因此,在选择模型时,不仅要考虑其准确性,还要考虑其推理速度和计算足迹,以确保它可以在时间敏感的临床环境中实际部署。
下表对所讨论的主要 AI 架构类别之间的关键权衡进行了高级综合。
表 2:先进 AI 去噪架构的综合比较
| 架构类别 | 示例模型 | 核心原理 | 训练范式 | 主要优势 | 显著弱点 |
| CNN | DnCNN, U-Net, ResNet | 卷积滤波器、残差学习、跳跃连接 | 监督式、自监督式 | 推理速度快、基准强大、技术成熟 | 感受野有限、难以处理全局上下文 |
| GAN | cGAN, WGAN | 对抗性训练(生成器 vs. 判别器) | 监督式、无监督式 | 卓越的感知质量、图像清晰 | 训练不稳定、有幻觉细节的风险 |
| Transformer | SwinIR, Imaging Transformer | 自注意力机制 | 监督式 | 卓越的全局上下文建模、在低信噪比下表现 SOTA | 计算密集(Swin 有所缓解)、较新的架构 |
| 扩散模型 | DDPM, Di-Fusion | 迭代去噪(反向扩散过程) | 监督式、自监督式 | SOTA 生成质量、高度逼真的纹理 | 推理速度非常慢、幻觉风险高、可能降低指标 |
| PINN | PIND | 物理信息损失函数 | 监督式、自监督式 | 鲁棒性高、保持定量准确性、更值得信赖 | 需要已知的物理模型、应用特定 |
第 8 节:从实验室到临床:挑战与未来展望
尽管在开发强大的 AI 去噪算法方面取得了显著进展,但从一篇成功的研究论文到广泛采用的临床工具的道路上充满了重大挑战。克服这些与鲁棒性、信任度和实际实施相关的障碍,将定义医学成像领域 AI 的未来。成功转化这些技术需要共同努力,超越在精选数据集上优化性能,转而构建可靠、可泛化和透明的系统。
8.1. “领域漂移”问题:泛化性和鲁棒性
AI 在临床上广泛采用的最大技术障碍是*“领域漂移”或“数据集漂移”*问题。[30] 一个 AI 模型,特别是用监督学习训练的模型,往往在与其训练数据相似的数据(“域内”)上表现出色,但在部署到来自不同来源的数据(“域外”)时可能会出现不可预测的失败。这种不匹配可能源于扫描仪制造商(例如,西门子 vs. GE vs. 飞利浦)、场强(1.5T vs. 3T)、采集协议、患者群体甚至软件版本的变化。[73] 一个在某个机构的公共数据集上产生最先进结果的 AI 模型,在另一家医院使用时可能不具备鲁棒性或可靠性,这种现象削弱了其临床效用。[30]
训练数据中的偏见加剧了这个问题。在小型或多样性不足的数据集上训练的模型几乎肯定无法捕捉到真实世界临床案例的巨大异质性,并且容易学习到特定于训练集的虚假关联。[30] 研究领域的碎片化,不同的研究使用不同的数据集和评估方法,使得真正评估新模型的泛化性变得困难。[73]
解决这一挑战是当前研究的主要焦点。关键策略包括:
在大型、多样化、多中心的数据集上进行训练,以使模型接触到更广泛的领域。[25, 44]
开发与供应商无关的解决方案,这些解决方案可以作为后处理工具应用于任何扫描仪的图像,通常通过避免依赖专有的原始 k 空间数据来实现。[25]
推进无监督和自监督学习方法,这些方法可以更容易地适应新的数据领域,因为它们不依赖于来自特定源领域的固定基准标签集。[52]
8.2. “黑箱”问题:可解释性和信任
为了让临床医生能够自信地将 AI 整合到他们的诊断工作流程中,他们必须能够信任其输出。阻碍这种信任的一个主要障碍是许多深度学习模型的“黑箱”性质。要理解一个复杂的网络为什么做出某个特定的决定——例如,为什么它平滑了某个区域或保留了某个特定的纹理——可能极其困难。[74] 这种缺乏透明度是临床采用的一个重要障碍。[75]
风险是巨大的。一个无法解释的模型可能会系统性地抹去细微但重要的病理特征,或者生成看似合理但实际上是伪影的结构,而用户却不清楚其原因。[74, 76] 如果不了解模型的失败模式,就无法安全地部署它。
这催生了可解释性 AI (XAI) 领域,该领域旨在开发技术,使模型的行为更加透明和易于人类理解。[75] 在去噪的背景下,这可能包括生成“显著性图”,突出显示输入图像的哪些部分对去噪输出影响最大。一个更强大的解决方案在于物理信息神经网络 (PINNs) 的范式。通过用已知的 MR 物理定律明确约束模型的行为,PINNs 在本质上更具可解释性和可信赖性。临床医生可以对一个保证产生与他们已经理解和信任的物理原理一致的输出的模型抱有更大的信心。[58]
8.3. 开源框架和供应商无关解决方案的作用
AI 去噪领域的快速创新得益于强大的开放科学文化。开源软件和大规模公共数据集的可用性对于确保研究的可重复性、实现公平的基准测试以及使社区能够在先前工作的基础上进行建设至关重要。[30, 66]
几个关键资源在这一进展中发挥了重要作用。像MONAI这样的框架,一个专门为医学成像开发的基于 PyTorch 的库,提供了一套标准化的数据处理、训练和评估工具。[77] 像TorchIO这样的数据处理库进一步简化了 3D 医学图像所需的复杂预处理流程。[77] 大型公共数据集的发布,最著名的是纽约大学朗格尼健康中心的fastMRI 数据集原始 k 空间数据,为开发和测试重建和去噪算法提供了一个共同的基础。[78] 此外,许多研究人员现在在 GitHub 等平台上发布他们模型的代码,允许其他人验证他们的结果并调整他们的架构。[7, 43, 50]
虽然开源工具加速了研究,但临床部署通常涉及由扫描仪供应商直接集成的商业解决方案(例如,飞利浦的 SmartSpeed AI,佳能的 dDLR)。[20, 79] 这些系统功能强大,但通常是专有的“黑箱”。一个并行且重要的趋势是开发与供应商无关的软件,这些软件可以作为后处理步骤应用于任何扫描仪的 DICOM 图像,这对于确保先进的 AI 工具能够为拥有多供应商设备的机构所用至关重要。[25]
下表为对 MRI 去噪感兴趣的研究人员和开发人员提供了关键开源资源列表。
表 3:MRI 去噪的关键开源实现和数据集
| 资源名称 | 类型 | 链接/参考 | 描述/相关性 |
| MONAI | 框架 | github.com/Project-MONAI/MONAI | 一个基于 PyTorch 的开源框架,用于医疗保健成像中的深度学习。提供标准化的预处理、训练和分析工具。[77] |
| DIPY | 库 | github.com/dipy/dipy | 一个用于分析 3D/4D+ 医学成像的 Python 库,重点关注弥散 MRI。包括去噪和处理方法。[80] |
| SwinIR | 模型实现 | github.com/JingyunLiang/SwinIR | Swin Transformer for Image Restoration 的官方 PyTorch 实现,一个用于去噪和其他任务的最先进模型。[43] |
| DnCNN | 模型实现 | github.com/cszn/DnCNN | 基础去噪卷积神经网络的官方实现(MATLAB/PyTorch)。[81] |
| fastMRI 数据集 | 数据集 | fastmri.med.nyu.edu | 一个大规模的脑部和膝关节 MRI 原始 k 空间数据集,对于训练和验证重建和去噪模型至关重要。[78] |
| TorchIO | 库 | github.com/fepegar/torchio | 一个用于在 PyTorch 中高效加载、预处理、增强和基于块采样的 3D 医学图像的 Python 库。[77] |
8.4. 未来的研究轨迹和未解决的问题
基于 AI 的 MRI 去噪领域是动态且迅速发展的。尽管取得了重大进展,但仍有几个关键挑战存在,这些挑战定义了未来研究最有希望的方向。
一个强大的趋势是开发更复杂的混合系统。未来可能不在于单一的“纯”架构,而在于智能组合,利用 CNNs 的局部特征提取、Transformers 的全局上下文建模以及物理信息学习的稳健约束。[40, 82]
一个关键且仍未完全解决的问题是不确定性量化。一个真正临床级的 AI 不仅应能生成去噪后的图像,还应能提供其自身置信度的度量。它应能生成一个“不确定性图”,突出显示其重建不太可靠的图像区域,从而提醒放射科医生对这些区域进行更仔细的审查。
另一个有希望的途径是多模态学习。MRI 扫描通常涉及获取多种对比度(例如,T1w、T2w、FLAIR、DWI)。未来的模型可以设计为利用这些不同对比度之间的互补信息,以实现比单独处理每种对比度更稳健的去噪。[75, 83]
最后,AI 的范围正在从纯粹的去噪扩展到同步伪影校正。下一代模型将旨在创建统一的框架,能够一次性校正噪声、运动伪影、吉布斯振铃和其他图像降级源。[84, 85, 86]
最终,该领域的轨迹表明,正在从纯粹以模型为中心的观点转向更加以数据为中心的观点。虽然更好的架构将继续出现,但未来最重要的突破可能来自于开发更好的数据采集、整理和学习策略。自监督学习的成功,巧妙地解决了“无基准数据”的问题,就是这一点的证明。未来在联邦学习(在保护隐私的同时对分散的、多样化的数据进行训练)、创建更大更全面的开放基准,以及从有限或不完美的数据中学习的新方法方面的工作,将与设计下一个新颖的神经网络层同样重要,甚至更重要。
第 9 节:结论与建议
人工智能在磁共振图像去噪中的应用已从一个有前途的研究概念转变为强大的临床现实。从经典滤波器到复杂深度学习架构的演变,从根本上改变了图像质量与采集速度之间的权衡,为更快、更高分辨率和更易于获得的 MRI 开辟了新的可能性。然而,AI 去噪的领域是复杂而微妙的,没有单一算法能在所有应用和评估标准中独占鳌头。确定“最佳”AI 去噪器是高度依赖于具体情况的。
9.1. 综合最新技术:哪种 AI 去噪方法是“最佳”的?
回答哪种 AI 方法是“最佳”的问题,需要将这个词分解为一系列不同且有时相互竞争的目标:
对于原始性能和推动信噪比边界: 目前在纯粹去噪能力方面,特别是在极低信噪比环境下,最先进的技术属于基于 Transformer 的架构。像专门的 Imaging Transformer 这样的模型已经展示出前所未有的能力,能够从信噪比低于 1.0 的图像中恢复出具有临床有效性的信息,这在以前被认为是不可想象的。[44, 45] 它们的优势在于有效建模全局上下文,使其成为那些以从最嘈杂的输入中最大化图像质量为主要目标的应用的先锋。
对于鲁棒性和定量准确性: 最有希望的新兴范式是物理信息神经网络(PINNs)。通过将 MR 信号形成的物理定律直接整合到学习过程中,PINNs 提供了一种强大的机制,以确保输出不仅视觉上干净,而且在定量上准确且物理上合理。[58] 对于像 DWI 或 T1 映射这样的定量模态,其中保持生物标志物准确性至关重要,PINNs 代表了构建可信赖和可靠模型的最直接途径。[58]
对于数据效率和实际部署: 开发和部署监督式 AI 的最大瓶颈是需要大量干净的基准数据,而这对于 MRI 来说是不可用的。自监督学习通过使模型能够仅使用嘈杂的临床数据进行训练,直接解决了这个问题。[52, 53] 对于希望在没有创建配对数据集负担的情况下,利用自有数据开发定制模型的研究人员和机构来说,自监督方法是最实用和可扩展的途径。
对于性能和成熟度的平衡: 设计良好的3D 卷积神经网络,特别是那些基于 U-Net 架构的网络,仍然是一个强大、成熟且广泛使用的标准。它们在性能和计算效率之间提供了稳健的平衡,并构成了许多成功的研究和商业系统的骨干。[25, 28] 虽然在原始性能方面可能不再是绝对的最新技术,但它们是一个经过验证和可靠的主力。
对于感知质量(附带警告):像 GANs 和扩散模型这样的生成模型在生成具有高感知质量、逼真纹理和锐利边缘的图像方面无与伦比。然而,这种能力伴随着一个重大且未解决的风险,即“幻化”出具有临床误导性的细节。[36, 37] 在其可靠性和保真度能够得到严格保证之前,必须在任何诊断环境中极其谨慎地使用它们。
9.2. 对研究人员和从业者的建议
基于这项全面的分析,我们提出以下建议,以指导未来的工作和临床应用:
对于研究人员:
关注与临床相关的挑战: 将焦点从标准基准测试中 PSNR 的增量提升转移到解决泛化性、可解释性和不确定性量化等关键挑战上。该领域需要能够适应领域漂移并能向最终用户传达其自身置信度的模型。
拥抱混合和受约束的模型: 未来最有希望的方向在于架构的智能组合。探索融合 CNNs、Transformers 和物理信息原理优势的混合模型。使用物理先验来约束强大的生成模型可能是安全释放其潜力的关键。
推广开放和标准化的基准测试: 为了超越“基准幻觉”,社区应致力于创建大规模、多中心、多供应商的公共数据集和标准化的评估协议。这对于实现公平、可重复的比较和真正衡量泛化性方面的进展至关重要。
对于临床从业者(放射科医生、医学物理学家):
评估超越指标: 在评估商业或研究性 AI 工具时,不要只看表面的 PSNR 和 SSIM 分数。坚持使用反映您患者群体和扫描仪协议的各种本地数据进行验证。
优先进行定性和定量验证: 验证的黄金标准是由多位专家放射科医生进行定性评估,以确认诊断质量得以保持或提高,并且没有引入伪影。对于定量成像序列(DWI、T1 映射等),必须验证 AI 工具是否保持了衍生生物标志物的准确性和精确性。
保持“信任但核实”的态度: 拥抱 AI 提高图像质量和工作流程效率的潜力,但要保持健康的临床怀疑态度。注意潜在的失败模式,特别是幻化或抹去病理的风险,并与开发人员和物理学家密切合作,确保 AI 工具经过严格测试并满足您临床实践的具体需求和安全标准。
参考文献
Noise and artifacts in MR images (Chapter 11) - Introduction to Functional Magnetic Resonance Imaging - Cambridge University Press, accessed July 17, 2025, https://www.cambridge.org/core/books/introduction-to-functional-magnetic-resonance-imaging/noise-and-artifacts-in-mr-images/0D06ED6766D1CF57386CCE556B99AEBB
Noise and filtration in magnetic resonance imaging - PMC - PubMed Central, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC2169200/
The Rician Distribution of Noisy MRI Data - PMC, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC2254141/
Image Denoising Using Non-Local Means (NLM) Approach in ..., accessed July 17, 2025, https://www.mdpi.com/2076-3417/10/20/7028
MR Acoustics - Questions and Answers in MRI, accessed July 17, 2025, https://www.mriquestions.com/whats-that-noise.html
Why are MRI scans so loud? - Radiating Hope - Cincinnati Children's Blog, accessed July 17, 2025, https://radiologyblog.cincinnatichildrens.org/whats-with-all-the-noise/
ocimakamboj/DnCNN: Image Denoising with Residual Learning - GitHub, accessed July 17, 2025, https://github.com/ocimakamboj/DnCNN
MRI denoising with a non-blind deep complex-valued convolutional neural network, accessed July 17, 2025, https://pubmed.ncbi.nlm.nih.gov/39523816/
Evaluation of MRI Denoising Methods Using Unsupervised Learning - Frontiers, accessed July 17, 2025, https://www.frontiersin.org/journals/artificial-intelligence/articles/10.3389/frai.2021.642731/full
How denoising algorithms can improve MRI image quality - News-Medical.net, accessed July 17, 2025, https://www.news-medical.net/whitepaper/20250117/How-denoising-algorithms-can-improve-MRI-image-quality.aspx
Convolutional Neural Network for MR Image Noise Removal, accessed July 17, 2025, https://www.csie.ntu.edu.tw/~fuh/personal/ConvolutionalNeuralNetworkforMRImageNoiseRemoval.pdf
Convolutional neural network denoising technique on MRI examination using parallel imaging grappa (Generalized autocalibrating p, accessed July 17, 2025, https://www.radiologypaper.com/article/view/386/7-2-8
Denoising diffusion weighted imaging data using convolutional neural networks | PLOS One, accessed July 17, 2025, https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0274396
Medical Image Denoising Techniques: A Review - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/publication/357876362_Medical_Image_Denoising_Techniques_A_Review
94 - Denoising MRI images (also CT & microscopy images) - YouTube, accessed July 17, 2025, https://www.youtube.com/watch?v=ur6pi3L98kk
Evaluation of MRI Denoising Methods Using Unsupervised Learning - PMC, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC8212039/
(PDF) From Classical to Deep Learning: A Systematic Review of Image Denoising Techniques - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/publication/382408601_From_Classical_to_Deep_Learning_A_Systematic_Review_of_Image_Denoising_Techniques
Overview of Research on Digital Image Denoising Methods - PMC - PubMed Central, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC12031399/
What is the best denoising algorithm for Brain mri images? - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/post/what_is_the_best_denoising_algorithm_for_Brain_mri_images
Validation of a Denoising Method Using Deep Learning–Based Reconstruction to Quantify Multiple Sclerosis Lesion Load on Fast FLAIR Imaging | American Journal of Neuroradiology, accessed July 17, 2025, https://www.ajnr.org/content/early/2022/07/28/ajnr.a7589
A Dynamic Network with Transformer for Image Denoising - MDPI, accessed July 17, 2025, https://www.mdpi.com/2079-9292/13/9/1676
MRI denoising using Deep Learning and Non-local averaging - arXiv, accessed July 17, 2025, https://arxiv.org/pdf/1911.04798
Heterogeneous window Transformer for image denoising - arXiv, accessed July 17, 2025, https://arxiv.org/html/2407.05709v2
A Deep Learning Framework for Denoising MRI Images using Autoencoders, accessed July 17, 2025, https://www.researchgate.net/publication/371562197_A_Deep_Learning_Framework_for_Denoising_MRI_Images_using_Autoencoders
image-domain deep-learning denoising technique for accelerated parallel brain MRI: prospective clinical evaluation | Radiology Advances | Oxford Academic, accessed July 17, 2025, https://academic.oup.com/radadv/article/1/3/umae022/7733581
(PDF) Boosting Magnetic Resonance Image Denoising With Generative Adversarial Networks - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/publication/351005323_Boosting_Magnetic_Resonance_Image_Denoising_With_Generative_Adversarial_Networks
A review of deep learning in medical imaging: Imaging traits, technology trends, case studies with progress highlights, and future promises - PMC, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC10544772/
Denoising of volumetric magnetic resonance imaging using multi-channel three-dimensional convolutional neural network with applications on fast spin echo acquisitions, accessed July 17, 2025, https://qims.amegroups.org/article/view/127018/html
Deep Learning Based Noise Reduction for Brain MR Imaging: Tests on Phantoms and Healthy Volunteers - PubMed Central, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC7553817/
AI in medical imaging grand challenges: translation from competition to research benefit and patient care - PubMed Central, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC10546459/
Generative Adversarial Networks: A Primer for Radiologists | RadioGraphics, accessed July 17, 2025, https://pubs.rsna.org/doi/full/10.1148/rg.2021200151
GANs with MRI Data - by Nandini Lokesh Reddy - Medium, accessed July 17, 2025, https://medium.com/@nandinilreddy/gans-with-mri-data-97e5f97f107c
How Artificial Intelligence Is Shaping Medical Imaging Technology: A Survey of Innovations and Applications - PMC, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC10740686/
RCA-GAN: An Improved Image Denoising Algorithm Based on Generative Adversarial Networks - MDPI, accessed July 17, 2025, https://www.mdpi.com/2079-9292/12/22/4595
Zero-shot Low-field MRI Enhancement via Denoising Diffusion Driven Neural Representation - MICCAI, accessed July 17, 2025, https://papers.miccai.org/miccai-2024/paper/3647_paper.pdf
A Critical Analysis of Diffusion Models for Medical Image Denoising - MICCAI, accessed July 17, 2025, https://papers.miccai.org/miccai-2024/paper/2146_paper.pdf
On Instabilities of Unsupervised Denoising Diffusion Models in Magnetic Resonance Imaging Reconstruction - arXiv, accessed July 17, 2025, https://arxiv.org/html/2406.16983v1
Comparative Analysis of Noise Reduction Techniques for Body Fluid Image Enhancement | Request PDF - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/publication/390219992_Comparative_Analysis_of_Noise_Reduction_Techniques_for_Body_Fluid_Image_Enhancement
A Generative Adversarial Network technique for high-quality super-resolution reconstruction of cardiac magnetic resonance images - PubMed, accessed July 17, 2025, https://pubmed.ncbi.nlm.nih.gov/34699953/
A Lightweight CNN-Transformer Implemented via Structural Re-Parameterization and Hybrid Attention for Remote Sensing Image Super-Resolution - MDPI, accessed July 17, 2025, https://www.mdpi.com/2220-9964/14/1/8
Zero-shot Low-field MRI Enhancement via Denoising Diffusion Driven Neural Representation | MICCAI 2024 - Open Access, accessed July 17, 2025, https://papers.miccai.org/miccai-2024/855-Paper3647.html
SwinIR: Image Restoration Using Swin Transformer - CVF Open Access, accessed July 17, 2025, https://openaccess.thecvf.com/content/ICCV2021W/AIM/papers/Liang_SwinIR_Image_Restoration_Using_Swin_Transformer_ICCVW_2021_paper.pdf
SwinIR: Image Restoration Using Swin Transformer (official repository) - GitHub, accessed July 17, 2025, https://github.com/JingyunLiang/SwinIR
Imaging Transformer for MRI Denoising: a Scalable Model ..., accessed July 17, 2025, https://www.microsoft.com/en-us/research/publication/imaging-transformer-for-mri-denoising-a-scalable-model-architecture-that-enables-snr1-imaging/
(PDF) Imaging Transformer for MRI Denoising: a Scalable Model Architecture that enables SNR << 1 Imaging - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/publication/390811985_Imaging_Transformer_for_MRI_Denoising_a_Scalable_Model_Architecture_that_enables_SNR_1_Imaging
Transformer-based deep learning denoising of single and multi-delay 3D arterial spin labeling - PubMed, accessed July 17, 2025, https://pubmed.ncbi.nlm.nih.gov/37849048/
(ISMRM 2024) Deep learning enabled MRI general denoising at 0.55T, accessed July 17, 2025, https://archive.ismrm.org/2024/0874.html
(ISMRM 2024) Denoising very low field magnetic resonance images using native noise modeling and deep learning, accessed July 17, 2025, https://archive.ismrm.org/2024/2801.html
(ISMRM 2024) Imaging transformer for MRI denoising with SNR unit training: enabling generalization across field-strengths, imaging contrasts, and anatomy, accessed July 17, 2025, https://archive.ismrm.org/2024/0654.html
This is the official implementation of our proposed SwinMR - GitHub, accessed July 17, 2025, https://github.com/ayanglab/SwinMR
Noise2Noise MRI for High-resolution Diffusion-weighted Imaging of the Brain: Deep Learning-based denoising without need for Highly Averaged Ground-truth Images - ISMRM, accessed July 17, 2025, https://cds.ismrm.org/protected/19MProceedings/PDFfiles/3392.html
(PDF) Self‐supervised learning for denoising of multidimensional MRI data - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/publication/381765764_Self-supervised_learning_for_denoising_of_multidimensional_MRI_data
Self-supervised learning for denoising of multidimensional MRI data, accessed July 17, 2025, https://pubmed.ncbi.nlm.nih.gov/38934408/
Deep Learning for Accelerated and Robust MRI Reconstruction: a Review - arXiv, accessed July 17, 2025, https://arxiv.org/html/2404.15692v1
Physics-informed deep neural network for image denoising - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/publication/375679544_Physics-informed_deep_neural_network_for_image_denoising
(PDF) Physics Informed Neural Network Enhanced Denoising for Atomic Resolution STEM Imaging - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/publication/387140834_Physics_Informed_Neural_Network_Enhanced_Denoising_for_Atomic_Resolution_STEM_Imaging
[Literature Review] A Physics-Informed Deep Learning Model for MRI Brain Motion Correction - Moonlight | AI Colleague for Research Papers, accessed July 17, 2025, https://www.themoonlight.io/en/review/a-physics-informed-deep-learning-model-for-mri-brain-motion-correction
Physics-informed neural networks for denoising high b-value ..., accessed July 17, 2025, https://pubmed.ncbi.nlm.nih.gov/40494002/
Physics-informed neural networks for enhancing medical flow magnetic resonance imaging: Artifact correction and mean pressure and Reynolds stresses assimilation - AIP Publishing, accessed July 17, 2025, https://pubs.aip.org/aip/pof/article-abstract/37/2/025194/3336391
A Physics-Informed Deep Learning Model for MRI Brain Motion Correction - PMC, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC11844622/
[1911.04798] MRI denoising using Deep Learning and Non-local averaging - arXiv, accessed July 17, 2025, https://arxiv.org/abs/1911.04798
A Hybrid Approach for CT Image Noise Reduction Combining Method Noise-CNN and Shearlet Transform - Biomedical and Pharmacology Journal, accessed July 17, 2025, https://biomedpharmajournal.org/vol17no3/a-hybrid-approach-for-ct-image-noise-reduction-combining-method-noise-cnn-and-shearlet-transform/
Ways of cheating on popular objective metrics: blurring, noise, super-resolution and others, accessed July 17, 2025, https://videoprocessing.ai/metrics/ways-of-cheating-on-popular-objective-metrics.html
Image Quality Assessment through FSIM, SSIM, MSE and PSNR—A Comparative Study - Journal of Computer and Communications - SCIRP, accessed July 17, 2025, https://www.scirp.org/journal/paperinforcitation?paperid=90911
Performance comparison of different denoising methods on three benchmarks., accessed July 17, 2025, https://www.researchgate.net/figure/Performance-comparison-of-different-denoising-methods-on-three-benchmarks_tbl1_368842181
Benchmarking Deep Learning-Based Low-Dose CT Image Denoising Algorithms - arXiv, accessed July 17, 2025, https://arxiv.org/html/2401.04661v2
Deep learning-based denoising image reconstruction of body magnetic resonance imaging in children - PMC - PubMed Central, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC12119730/
(PDF) Evaluating Second-Generation Deep Learning Technique for Noise Reduction in Myocardial T1-Mapping Magnetic Resonance Imaging - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/publication/391890473_Evaluating_Second-Generation_Deep_Learning_Technique_for_Noise_Reduction_in_Myocardial_T1-Mapping_Magnetic_Resonance_Imaging
Evaluating Second-Generation Deep Learning Technique for Noise Reduction in Myocardial T1-Mapping Magnetic Resonance Imaging - PMC, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC12110243/
Accelerating Whole-Body Diffusion-weighted MRI with Deep Learning–based Denoising Image Filters - PubMed Central, accessed July 17, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC8489468/
(PDF) Comparative Study of Traditional and Deep-Learning Denoising Approaches for Image-Based Petrophysical Characterization of Porous Media - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/publication/358088510_Comparative_Study_of_Traditional_and_Deep-Learning_Denoising_Approaches_for_Image-Based_Petrophysical_Characterization_of_Porous_Media
Comparative Study of Traditional and Deep-Learning Denoising Approaches for Image-Based Petrophysical Characterization of Porous Media - Frontiers, accessed July 17, 2025, https://www.frontiersin.org/journals/water/articles/10.3389/frwa.2021.800369/full
Enhancing Radiologist Productivity with Artificial Intelligence in Magnetic Resonance Imaging (MRI): A Narrative Review - MDPI, accessed July 17, 2025, https://www.mdpi.com/2075-4418/15/9/1146
Challenges of deep learning in medical image analysis – improving explainability and trust - CentAUR, accessed July 17, 2025, https://centaur.reading.ac.uk/109789/1/Challenges%20of%20Deep%20Learning%20in%20Medical%20Image%20Analysis%20%E2%80%93%20Improving%20Explainability%20and%20Trust%20_%20Full%20Text.pdf
AI-Powered Object Detection in Radiology: Current Models, Challenges, and Future Direction - MDPI, accessed July 17, 2025, https://www.mdpi.com/2313-433X/11/5/141
Clinical Impact of Deep Learning Reconstruction in MRI | RadioGraphics - RSNA Journals, accessed July 17, 2025, https://pubs.rsna.org/doi/full/10.1148/rg.220133
kondratevakate/mri-deep-learning-tools - GitHub, accessed July 17, 2025, https://github.com/kondratevakate/mri-deep-learning-tools
mrphys/sodium_MRI_DnCNN: Example code for training a denoising convolutional neural network (DnCNN) for MRI - GitHub, accessed July 17, 2025, https://github.com/mrphys/sodium_MRI_DnCNN
Deep learning denoising reconstruction for improved image quality in fetal cardiac cine MRI, accessed July 17, 2025, https://www.frontiersin.org/journals/cardiovascular-medicine/articles/10.3389/fcvm.2024.1323443/full
denoising · GitHub Topics, accessed July 17, 2025, https://github.com/topics/denoising
cszn/DnCNN: Beyond a Gaussian Denoiser: Residual Learning of Deep CNN for Image Denoising (TIP, 2017) - GitHub, accessed July 17, 2025, https://github.com/cszn/DnCNN
A Review of Electromagnetic Elimination Methods for low-field portable MRI scanner - arXiv, accessed July 17, 2025, https://arxiv.org/html/2406.17804v1
A Systematic Review and Identification of the Challenges of Deep Learning Techniques for Undersampled Magnetic Resonance Image Reconstruction - MDPI, accessed July 17, 2025, https://www.mdpi.com/1424-8220/24/3/753
Deep learning methods for 3D magnetic resonance image denoising, bias field and motion artifact correction: a comprehensive review - PubMed, accessed July 17, 2025, https://pubmed.ncbi.nlm.nih.gov/39569887/
Using Deep Learning to Simultaneously Reduce Noise and Motion Artifacts in Brain MR Imaging - J-Stage, accessed July 17, 2025, https://www.jstage.jst.go.jp/article/mrms/advpub/0/advpub_mp.2024-0098/_article
(PDF) Deep learning methods for 3D magnetic resonance image denoising, bias field and motion artifact correction: a comprehensive review - ResearchGate, accessed July 17, 2025, https://www.researchgate.net/publication/386023151_Deep_learning_methods_for_3D_magnetic_resonance_image_denoising_bias_field_and_motion_artifact_correction_a_comprehensive_review